Adénocarcinome pancréatique : Traitements péri-opératoires
Service de Gastro-entérologie, Groupe des tumeurs Hépato-bilio-pancréatiques
Institut Roi Albert II, Cliniques universitaires St Luc
En association avec nos hôpitaux partenaires : Clinique St Jean (Bruxelles), Clinique St Pierre (Ottignies), Clinique ND de Grâce (Gosselies)
Introduction
Comme l’a rappelé le Dr Catherine Hubert dans son article, (lire ici) le cancer du pancréas est difficile à traiter de par son diagnostic malheureusement souvent tardif, la complexité de la chirurgie et la - relative - inefficacité des traitements non chirurgicaux. Nous allons cependant nuancer ce tableau et espérons vous convaincre de l’indispensable interactivité entre les différents spécialistes et le médecin généraliste pour traiter adéquatement de manière multimodale les patients atteints de cancers du pancréas.
Un diagnostic et une stadification correcte pour un traitement optimal
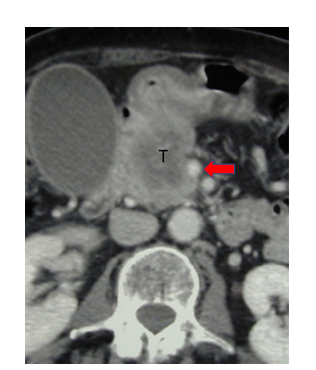
Au sein du groupe des tumeurs Hépato-bilio-pancréatiques, nous apportons beaucoup d’importance au diagnostic et à une stadification très précise dans tous les cas de figures, donc aussi bien pour les tumeurs locales que localement avancées ou métastatiques. Pour ces dernières, bien souvent un scanner suffira à objectiver une extension métastatique, le plus souvent dans le foie mais aussi dans les poumons et le péritoine. Il nous semble opportun d’insister sur deux critères pour cet examen, car le médecin traitant est souvent le premier à le prescrire : afin de bien voir une tumeur dans le pancréas, il est indispensable de réaliser un scanner spiralé avec injection et de demander 3 temps : artériel, veineux et tardif. Sans produit de contraste, une tumeur est rarement visible et l’examen est donc non seulement inutile, mais faussement rassurant. Les 3 temps de l’examen permettent, surtout pour les tumeurs non métastatiques, de décrire les contacts vasculaires, tant veineux qu’artériels, indispensables pour le pronostic mais aussi et surtout pour la prise en charge. A titre d’exemple, la figure 1 vous montre une image obtenue par scanner injecté triphasique, d’une tumeur de la tête du pancréas (T) présentant un contact intime avec le tronc coeliaque émergeant de l’aorte (flèche rouge). Cette tumeur est par conséquent définie comme une tumeur localement avancée, mais chirurgicalement irrésécable de manière curative même par l’équipe chirurgicale la plus compétente.
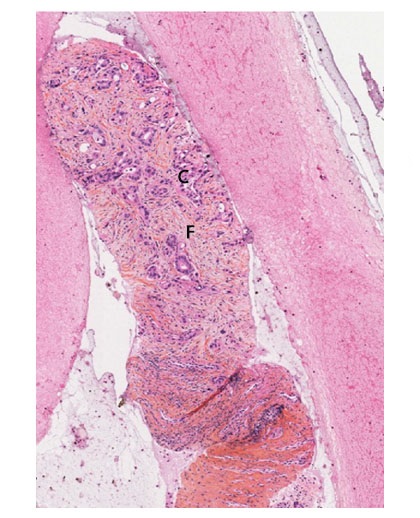
Nous réalisons pour tous les patients une ponction-biopsie, soit par voie percutanée en cas de métastase hépatique par exemple, soit par voie écho-endoscopique pour les tumeurs non métastatiques.
A l’Institut Roi Albert II des Cliniques universitaires Saint-Luc, nous avons été pionniers dans cette technique endoscopique qui permet de donner un diagnostic de certitude dans plus de 97% des cas. De plus, à l’ère des traitements personnalisés et de l’immunothérapie, il n’est plus suffisant de « juste » affirmer qu’il s’agit d’un adénocarcinome, mais il faut également être capable de fournir assez de tissu tumoral pour que nos collègues anatomo-pathologistes puissent réaliser des examens complémentaires, y compris des analyses moléculaires plus poussées. En effet, même si ce n’est pas encore important dans notre pratique quotidienne, ces analyses deviendront essentielles dans un proche avenir évoluant vers des traitements personnalisés. La figure 2 vous montre un prélèvement obtenu par écho-endoscopie en 2020. On observe les cellules cancéreuses («C») au sein du tissu péri-tumoral fibreux («F»)
Un traitement multi-modal adapté à chaque situation
Adénocarcinomes métastatiques
Dans cette situation qui concerne malheureusement encore près de 50% des patients au diagnostic, le traitement exclusif est la chimiothérapie. Trois types de protocoles thérapeutiques peuvent être proposés : pour les patients ayant peu de symptômes, en bon état général, âgés de moins de 70 ans, le schéma « FOLFIRINOX » est proposé, qui combine le 5-fluorouracile (5-FU), l’irinotecan et l’oxaliplatine. C’est une chimiothérapie lourde, que l’on propose de maintenir pendant 6 mois. Il arrive fréquemment que les doses soient adaptées, et l’oxaliplatine est régulièrement interrompue après 4 mois, en raison de sa neurotoxicité. Aux laboratoire des Cliniques universitaires Saint-Luc, l’équipe du Dr Vincent Haufroid a été pionnière en Belgique dans le développement d’un test sanguin qui permet de prédire la toxicité du 5-FU liée à un déficit génétique de l’enzyme qui dégrade la molécule, la dihydropyrimidine déshydrogénase (DPD). Une minorité de patients (3-8%) présentent en effet un déficit partiel en DPD qui peut mener à des effet secondaires graves si l’on administre 100% de la dose théorique de 5-FU. Quant au déficit complet en DPD (0,05-0,1% de la population), il peut entrainer jusqu’à des décès en cas d’administration. Nous réalisons donc ce test chez tous les patients qui vont commencer cette chimiothérapie. Une autre association efficace est la combinaison de gemcitabine et de nab-paclitaxel, qui peut être administrée à des patients plus fragiles, plus âgés mais encore en bon état général, car elle donne moins d’effets secondaires, mais potentiellement aussi une efficacité moindre. Enfin, pour les patients très affaiblis, il est important de discuter avec eux, en alternative à la chimiothérapie, de l’opportunité de mettre en place des soins de support/confort. Last but not least, nous pouvons très régulièrement proposer des protocoles de recherche avec des nouveaux produits qui ciblent par exemple le métabolisme énergétique, l’environnement fibreux souvent très dense dans le cancer du pancréas.
Adénocarcinomes localement avancés
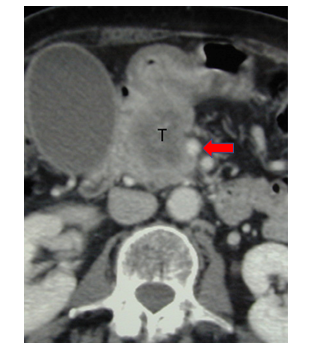
La catégorie de patients qui ne présentent pas de métastases, mais une tumeur avec des contacts vasculaires qui la rendent inopérable (Figure 1), fait l’objet d’intenses discussions en réunion pluridisciplinaire. La proposition de traitement est la chimiothérapie « FOLFIRINOX » lorsque les patients sont en bon état général. En effet, les diminutions de taille ne sont pas rares, permettant, plus rarement il est vrai, de reconsidérer la chirurgie qui devra toutefois rester un traitement d’exception. Pour ces patients, le bilan initial comprendra alors également un PET-CT au FDG, qui servira surtout de marqueur métabolique d’efficacité ; en effet lorsque la captation de FDG (glucose radioactif) diminue ou disparaît en cours de traitement, cela témoigne d’une bonne efficacité. Le dossier du patient est régulièrement présenté en Consultation Oncologique Multidisciplinaire (COM), et l’option chirurgicale (résécabilité à visée curative) est toujours rediscutée. En général, après 4 mois de chimiothérapie, si la tumeur n’est pas opérable, on propose soit une pause thérapeutique, soit une radiothérapie. La survie attendue avec cette stratégie thérapeutique est en médiane de 12 à 18 mois.
Adénocarcinomes potentiellement résécables
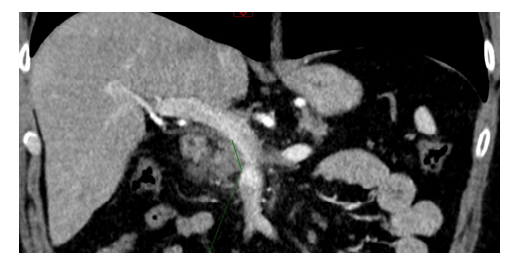
Il s’agit de patients présentant un contact vasculaire moins prononcé, en général sur la veine Porte ou le confluent porto-mésentérique (Figure 3). En théorie, ce sont des patients que l’on pourrait opérer d’emblée, mais notre équipe a démontré il y a déjà plus de 10 ans que le pronostic était nettement moins bon avec une chirurgie première parce que la récidive était beaucoup plus fréquente (1). C’est pour ces patients que les efforts maximaux sont mis en place afin de les rendre résécables. En principe, nous utilisons le même schéma FOLFIRINOX car c’est le plus efficace en termes de diminution tumorale (environ 30% de réponses), permettant surtout un taux élevé de chirurgie (67%) et une survie médiane de 22 mois, assez similaire à la survie de patients opérés d’emblée pour des tumeurs résécables d’emblée, bien sûr (2). Une durée de 2 à 4 mois de traitement est nécessaire, avec en fonction de la réponse, un usage au cas par cas de la radiothérapie. La même philosophie de ré-évaluation régulière est de mise, comme pour les tumeurs localement avancées.
Adénocarcinomes résécables
Ces patients sont opérés d’emblée par notre équipe chirurgicale, et s’ils ont récupéré correctement de l’intervention, bénéficient de chimiothérapie adjuvante, selon le schéma FOLFIRINOX (voir l’article du Dr Hubert dans ce même numéro).
Un effort francophone d’harmonisation des pratiques, le registre « NEOPAC »
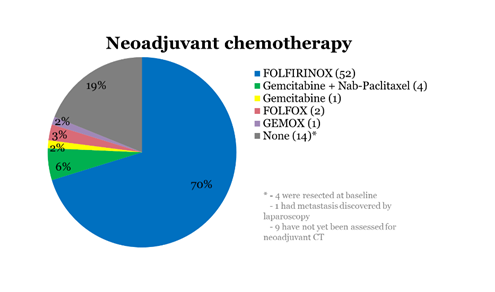
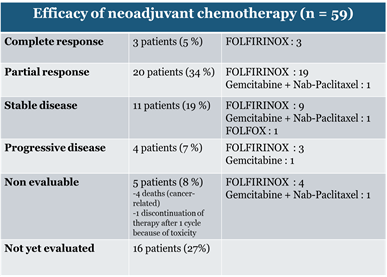
Il y a 3 ans de cela, nous avons initié, avec le CHU Sart-Tilman, les hôpitaux de liège, et l’hôpital ULB-Erasme, une étude prospective observationnelle, le registre NEOPAC, dont le but est d’enregistrer et d’harmoniser les pratiques diagnostiques et thérapeutiques des patients atteints de cancers du pancréas non métastatiques. À ce jour, 125 patients sont inclus dans le registre, dont environ 30% suivis et traités à Saint-Luc. Les données ont été communiquées à deux reprises au congrès national de gastroentérologie (www.bwge.be) par le Dr Siplet, dont c’était le travail de fin d’études. Le Dr Siplet est gastroentérologue à la Clinique Saint-Pierre d’Ottignies, et sa présence permet de poursuivre un fructueux partenariat dont les patients sont les premiers bénéficiaires. Les figures 4 et 5 vous montrent que les chimiothérapies sont très similaires entre centres, et que les résultats sont encourageants. L’effort se poursuit, et une publication scientifique paraitra prochainement, détaillant nos résultats.
Références
- Ouaissi M, Hubert C, Verhelst R, Astarci P, Sempoux C, Jouret-Mourin A, et al. Vascular reconstruction during pancreatoduodenectomy for ductal adenocarcinoma of the pancreas improves resectability but does not achieve cure. World J Surg. 2010;34(11):2648-61.
- Lambert A, Schwarz L, Borbath I, Henry A, Van Laethem JL, Malka D, et al. An update on treatment options for pancreatic adenocarcinoma. Ther Adv Med Oncol. 2019;11:1758835919875568.
